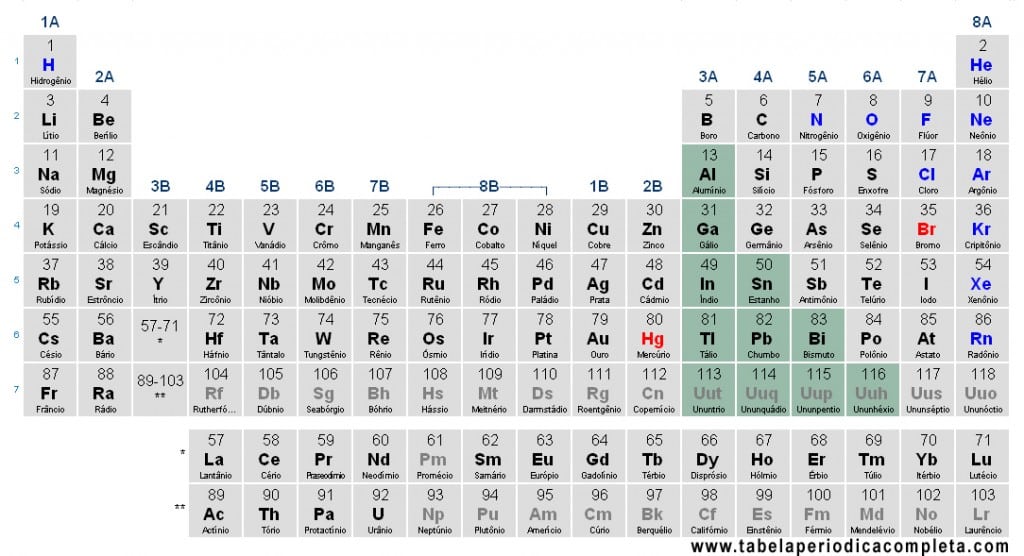
Os Metais Representativos são os metais localizados nos blocos s e p da Tabela Periódica (grupos 1, 2 e os metais dos grupos 13–16). Diferem dos metais de transição (bloco d) porque sua configuração eletrônica de valência termina em ns1–2 ou ns2np1–4, o que explica boa parte de suas propriedades químicas.
Configuração eletrônica dos representativos (visão didática)
Nos elementos representativos, o último nível apresenta a seguinte distribuição eletrônica de valência:
- ns¹ → grupo 1 (metais alcalinos)
- ns² → grupo 2 (metais alcalino-terrosos)
- ns²np¹–np4 → metais do bloco p (grupos 13–16). Obs.: grupos 17–18 são majoritariamente não-metais/nobres e, portanto, não entram na lista de metais representativos.
Quais são os Metais Representativos (bloco p)
Além dos grupos 1 e 2 (todos metálicos), os metais do bloco p que compõem os Metais Representativos incluem:
- Alumínio (Al)
- Gálio (Ga)
- Índio (In)
- Tálio (Tl)
- Estanho (Sn)
- Chumbo (Pb)
- Bismuto (Bi)
- Polônio (Po) (metal do grupo 16)
- Nihônio (Nh) – ex-Uut (Z = 113)
- Fleróvio (Fl) – ex-Uuq (Z = 114)
- Moscóvio (Mc) – ex-Uup (Z = 115)
- Livermório (Lv) – ex-Uuh (Z = 116)
Nota de nomenclatura: os antigos nomes temporários Ununtrio (Uut), Ununquádio (Uuq), Ununpentio (Uup) e Ununhéxio (Uuh) foram oficialmente substituídos por Nihônio (Nh), Fleróvio (Fl), Moscóvio (Mc) e Livermório (Lv). São elementos sintéticos, de meia-vida muito curta e com propriedades experimentais ainda limitadas.
Propriedades gerais e tendências periódicas
- Caráter metálico aumenta ao descer nos grupos e diminui da esquerda para a direita no período.
- Estados de oxidação típicos: Al (+3); Ga/Ín/Tl (+1/+3, efeito do par inerte favorece +1 nos mais pesados); Sn/Pb (+2/+4, com preferência crescente por +2 em Pb); Bi (+3/+5, com +3 mais estável); Po (+2/+4, podendo atingir +6).
- Reatividade: alcalinos e alcalino-terrosos são muito reativos; no bloco p a reatividade varia conforme raio, eletronegatividade e efeito de blindagem.
- Anfoterismo: Al(OH)₃ e Sn(OH)₂/Sn(OH)₄ exibem comportamento anfótero; Pb(OH)₂ também.
- Ligação e estrutura: muitos formam óxidos, haletos, hidróxidos e complexos com diferentes coordenações.
Exemplos, compostos e aplicações
- Alumínio (Al): leve, resistente à corrosão (camada de Al₂O₃); uso em ligas, embalagens, construção e condução elétrica.
- Gálio (Ga) e Índio (In): ligas de baixo ponto de fusão, semicondutores (GaAs, InP), telas (ITO – óxido de índio-estanho).
- Tálio (Tl): semicondutores específicos e dispositivos ópticos; tóxico, exige controle rigoroso.
- Estanho (Sn): ligas (soldas, bronze), revestimentos anticorrosivos (estanhagem), catalisadores e estabilizantes de PVC.
- Chumbo (Pb): baterias chumbo–ácido, blindagens radiológicas; composto de Pb(II) requer gestão ambiental devido à toxicidade.
- Bismuto (Bi): baixa toxicidade relativa; fármacos (subsalisilato), ligas de fusão, catalisadores.
- Polônio (Po): radioativo, uso restrito (fontes de calor e ionização em aplicações especiais).
Metais representativos × Metais de transição
Embora cobre (Cu) e zinco (Zn) exibam algumas semelhanças em propriedades periódicas, são metais de transição do bloco d, não integrantes dos metais representativos. O critério que prevalece é a ocupação do subnível d no estado fundamental/estados de oxidação estáveis.
Boas práticas e aspectos ambientais
Alguns metais representativos e seus compostos exigem cuidados: Pb e Tl são tóxicos; compostos de Sn organoestânicos requerem controle; Po é radiotóxico. É fundamental cumprir normas de segurança química, descarte e substituição por alternativas menos perigosas quando aplicável.
FAQ – Perguntas Frequentes sobre Metais Representativos
Quais grupos formam os Metais Representativos?
Correspondem aos blocos s e p da tabela: todos os metais dos grupos 1 e 2 (alcalinos e alcalino-terrosos) e os metais dos grupos 13–16 (p-bloco).
Por que alguns elementos têm dois estados de oxidação estáveis?
Devido a fatores como efeito do par inerte, tamanho do íon, blindagem e estabilidade eletrônica; por exemplo, Sn (+2/+4) e Pb (+2/+4) mostram preferência crescente por +2 nos mais pesados.
Os nomes Ununtrio/Uuq/Uup/Uuh ainda estão corretos?
Não. As denominações oficiais são Nihônio (Nh), Fleróvio (Fl), Moscóvio (Mc) e Livermório (Lv). São sintéticos e de meia-vida curta.
Metais representativos formam compostos anfóteros?
Sim, alguns como Al, Sn e Pb têm hidróxidos anfóteros, reagindo tanto com ácidos quanto com bases.
Qual a principal diferença para os metais de transição?
Os representativos têm valência terminando em s ou p, com química mais previsível por carga do cátion e tamanho; os de transição (bloco d) exibem múltiplos estados de oxidação e rica química de coordenação d.